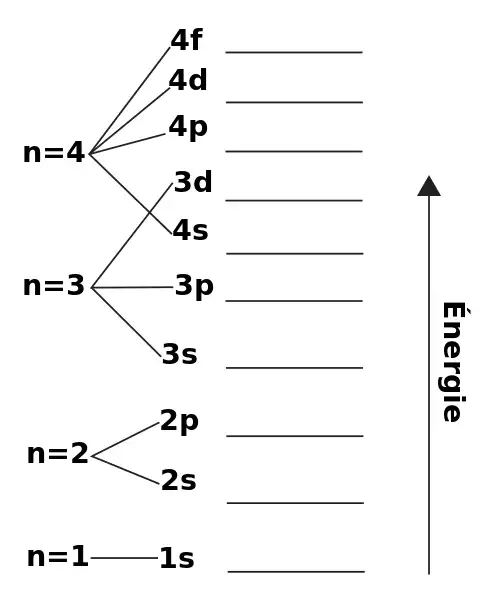
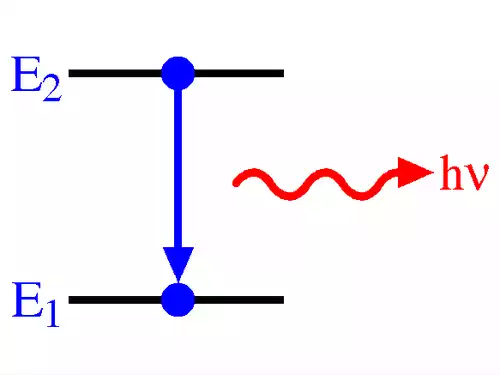
تراز انرژی
معنی کلمه تراز انرژی در دانشنامه عمومی
اگر انرژی پتانسیل در فاصلهٔ بینهایت از هستهٔ اتم یا مولکول صفر باشد، در این حالت الکترون های ثابت ( به انگلیسی: Bound state ) دارای پتانسیل منفی خواهند بود.
اگر بیش از یک حالت کوانتومی کلاسیک انرژی برابر با هم داشته باشند، اصطلاحاً گفته می شود که ترازهای انرژی رو به انحطاط گذارده اند که منجر به ایجاد چندگانگی می شود.
تبهگنی یا واگنگی ( Degenerate ) : اگر به یک تراز انرژی، دو یا چند تابع موج متمایز، متناظر شود می گوییم تراز انرژی تبهگن است.
برای مثال:اگر ( n=n ( 1 ) +n ( 2 و E ( n ) = ( n+1 ) h*w به ازای ( n ( 1 ) =۱ و n ( 2 ) =۰ ) یا ( n ( 1 ) =۰ و n ( 2 ) =۱ ) تنها یک مقدار انرژی E=۲*h*w بدست می دهد ولی دو تابع متفاوت حاصل می شود، لذا این تراز انرژی تبهگنی دوگانه دارد.
ترازهای انرژی تدریجی حاصل رابطهٔ میان انرژی ذره ها و طول موج آن ها است. این رابطه نخستین بار در سال ۱۸۰۰ مشاهده شد و توسط نیلز بور دانشمند دانمارکی در سال ۱۹۱۳ ثبت شد و در سال ۱۹۲۶ توسط دو دانشمند آلمانی کامل گشت.
با تصور الکترونی که درون اتم هیدروژن به دور هسته می چرخد. انرژی این الکترون از تأثیر الکترواستاتیکی الکترون منفی و هستهٔ مثبت به دست می آید. تراز انرژی الکترون دور هسته از رابطهٔ زیر به دست می آید:
( معمولاً بین ۱ eV and 10۳ eV )
•
• R ∞ {\displaystyle R_{\infty }\ } is the ثابت ریدبرگ
• Z is the عدد اتمی
• n is the اعداد کوانتومی اصلی
• h {\displaystyle h} is ثابت پلانک
• c is the سرعت نور
برای اتم ها یا یون ها یی مشابه با هیدروژن تراز ریدبرگ تنها به اعداد کوانتومی اصلی ( n ) بستگی دارد.
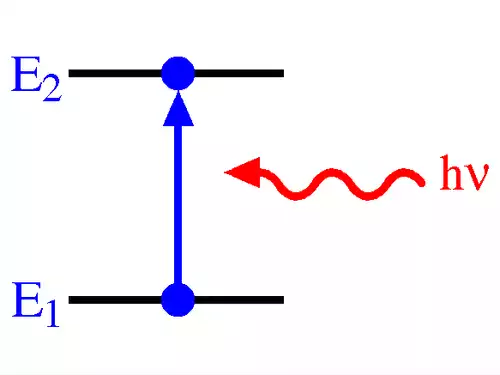
معنی کلمه تراز انرژی در دانشنامه آزاد فارسی
انرژی مجاز الکترون، در هر اتم خاص. ترازهای انرژی را به کمک نظریۀ کوانتومی محاسبه می کنند. ترازهای انرژی مجاز عمدتاً به فاصلۀ بین الکترون و هسته وابسته اند.
معنی کلمه تراز انرژی در ویکی واژه
جملاتی از کاربرد کلمه تراز انرژی
تراز انرژی هیدروژن را میتوان با کمک مدل اتمی بور، با تقریب خوبی بهدستآورد. در مدل بور فرض بر این است که الکترونها در اتم، مانند زمین که به گِرد خورشید میگردد، به گِرد پروتون (هستهٔ اتم) میچرخند. البته نیروی الکترومغناطیسی میان الکترونها و پروتونها ربایش پدیدمیآورد مانند سیارهها که به خاطر نیروی گرانش سوی ستارهها رباییده میشوند. در دوران آغازین مکانیک کوانتوم چنین انگار شده بود که تکانهٔ زاویهای کمیتی گسسته است در نتیجه الکترون در مدل بور اجازه داشت در فاصلههای مشخصی از پروتون جای گیرد و در نتیجه انرژی آن هم با مقدارهای مشخصی برابر میشد.
تراز انرژی الکترون در اتم هیدروژن، در پایینترین سطح خود یا حالت صفر، ۱۳٫۶- الکترونولت است؛ که برابر است با یک فوتون فرابنفش با طول موجی نزدیک به ۹۲ نانومتر.
در ۱۹۱۴ نیلز بور با در نظر گرفتن چند فرض سادهکننده توانست بسامدهای طیفی هیدروژن را بدست آورد. فرضهایی که بور کرد پایهٔ مدل بور بود. همهٔ این فرضها درست نبود اما در نهایت بور را به مقدار انرژی درستی رساند. در سالهای ۱۹۲۵ تا ۱۹۲۶ درستی نتایج بور در بسامدها و ترازهای انرژی، توسط مکانیک کوانتوم و با بهرهگیری از معادلهٔ شرودینگر نشان داده شد. معادلهٔ شرودینگر تراز انرژی هیدروژن و از آن بسامدهای خطهای طیفی هیدروژن را محاسبه میکرد. همچنین با کمک این معادله میشد تابع موج الکترونها (ابر الکترونی) را هم برای چندین حالت کوانتومی بهدست آورد و در نتیجهٔ آن برای ویژگی ناهمسانگردی پیوندهای اتمی توضیحی پیدا کرد، چیزی که مدل بور در آن ناتوان بود.
در دماهای پایین، رفتار بوزونها با فرمیونها که از آمار فرمی-دیراک تبعیت میکنند متفاوت است. از این جهت که تعداد نامحدودی از بوزونها میتوانند در یک تراز انرژی چگالیده شوند. این ویژگی منجر به چگالش بوز-اینشتین (حالتی خاص از ماده) میگردد. آمارهای بوز-اینشتین و فرمی-دیراک، آمارهای کوانتومی هستند، یعنی تنها در شرایط دمای پایین و چگالی بالا که آثار کوانتومی قابل توجه هستند اعمال میگردند.