الکترون ظرفیت
معنی کلمه الکترون ظرفیت در دانشنامه عمومی
برای یک عنصر از گروه اصلی، الکترون ظرفیت، تنها می تواند در بیرون ترین قسمت پوستهٔ بیرونی الکترون وجود داشته باشد. در یک فلز واسطه، الکترون ظرفیت می تواند در یک پوستهٔ داخلی نیز قرار داشته باشد.
اتمی که لایه های الکترونی ظرفیت آن بسته باشد؛ ( وابسته به آرایش پیکربندی الکترونی s²p⁶ ) ، از نظر شیمیایی تمایلی به پیوند ندارد و نسبت به دیگر اتم ها «بی اثر» است. اتم های دارای یک یا دو الکترون ظرفیت اضافی در یک لایهٔ بسته، به دلیل داشتن انرژی نسبتاً کم برای خارج ساختن الکترون های اضافی برای ایجاد یون مثبت، بسیار واکنش پذیر هستند. اتمی با کمبود یک یا دو الکترون در یک لایهٔ بسته، به دلیل تمایل آن برای به دست آوردن الکترون های از دست رفته و تشکیل یون منفی، یا در غیر این صورت برای به اشتراک گذاشتن الکترون های ظرفیتی و تشکیل پیوند کووالانسی، واکنش پذیر است.
همانند یک الکترون موجود در پوستهٔ داخلی، یک الکترون ظرفیت نیز توانایی جذب یا آزادسازی انرژی به شکل فوتون را دارد. دریافت انرژی اضافی می تواند باعث شود تا الکترون به لایهٔ بیرونی تری جهش کند. این پدیده به حالت برانگیخته معروف است. در این حالت، اگر الکترون انرژی کافی برای غلبه بر سد بالقوه ای که برابر با پتانسیل یونیزاسیون است دریافت کند، الکترون حتی می تواند اتم را ترک و آزاد شود و بنابراین، یک یون مثبت را تشکیل دهد. در شرایطی که الکترون انرژی خود را با انتشار یک فوتون از دست می دهد، می تواند درون یک لایهٔ داخلی که کاملاً اشغال نشده حرکت کند.
سطح انرژی ظرفیت با اعداد کوانتومی اصلی ( n = ۱، ۲ ، ۳، ۴ ، ۵ . . . ) مطابقت داده می شوند، یا با حروف الفبا، با حروف مورد استفاده در نماد پرتو ایکس: ( K , L، M ، . . . ) ، برچسب زده می شوند.
معنی کلمه الکترون ظرفیت در دانشنامه آزاد فارسی
در شیمی، الکترونِ خارجی ترین لایۀ هر اتم. الکترون های ظرفیت در تشکیل پیوندهای کووالانسی و یونی درگیر می شوند (← مولکول). تعداد الکترون ها در لایۀ خارجی بیشترین ظرفیتِ ممکن را برای بسیاری از عناصر نشان می دهد و شمارۀ گروهی را معین می کند که این عنصر در جدول تناوبی عناصر اشغال کرده است.
جملاتی از کاربرد کلمه الکترون ظرفیت
همانند یک الکترون موجود در پوستهٔ داخلی، یک الکترون ظرفیت نیز توانایی جذب یا آزادسازی انرژی به شکل فوتون را دارد. دریافت انرژی اضافی میتواند باعث شود تا الکترون به لایهٔ بیرونیتری جهش کند. این پدیده به حالت برانگیخته معروف است. در این حالت، اگر الکترون انرژی کافی برای غلبه بر سد بالقوهای که برابر با پتانسیل یونیزاسیون است دریافت کند، الکترون حتی میتواند اتم را ترک و آزاد شود و بنابراین، یک یون مثبت را تشکیل دهد. در شرایطی که الکترون انرژی خود را با انتشار یک فوتون از دست میدهد، میتواند درون یک لایهٔ داخلی که کاملاً اشغال نشده حرکت کند.
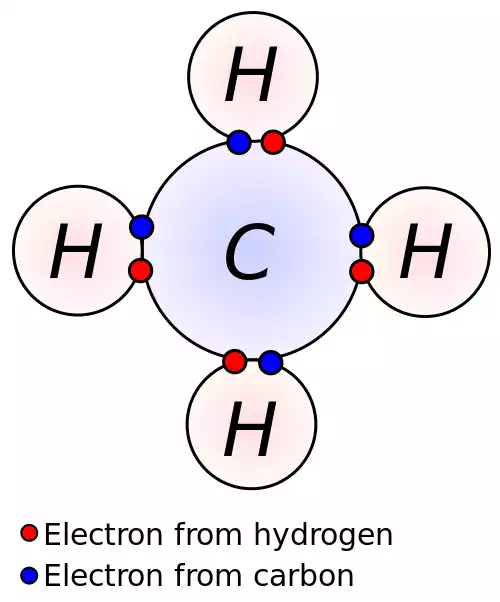
در دانش شیمی، الکترون ظرفیت یک الکترون وابسته به الکترونهای پوسته یا لایه الکترونی یک اتم است و اگر پوستهٔ بیرونی بسته نباشد، این الکترون میتواند در ایجاد و تشکیل یک پیوند شیمیایی شرکت کند. در یک پیوند کووالانسی (تک والانسی)، هر دو اتم درگیر در پیوند به منظور تشکیل یک پیوند کووالانسی، هرکدام یک الکترون ظرفیت عرضه میکنند. رفتار یک عنصر شیمیایی در واکنشهای شیمیایی با حضور و شمار الکترونهای ظرفیت تعیین میشود. خواص شیمیایی هر عنصر را الکترونهای ظرفیت تعیین میکند مانند: ویژگی ظرفیت شیمیایی آن - و اینکه آیا ممکن است به دیگر عنصرها بپیوندد یا نه؛ و اگر چنین است، میزان آمادگی و با چند الکترون؟
توضیح پیچیده تر از تفاوت میان هسته و الکترون ظرفیت را می توان با نظریه مداری بیان کرد.
برای یک عنصر از گروه اصلی، الکترون ظرفیت، تنها میتواند در بیرونترین قسمت پوستهٔ بیرونی الکترون وجود داشتهباشد. در یک فلز واسطه، الکترون ظرفیت میتواند در یک پوستهٔ داخلی نیز قرار داشتهباشد.
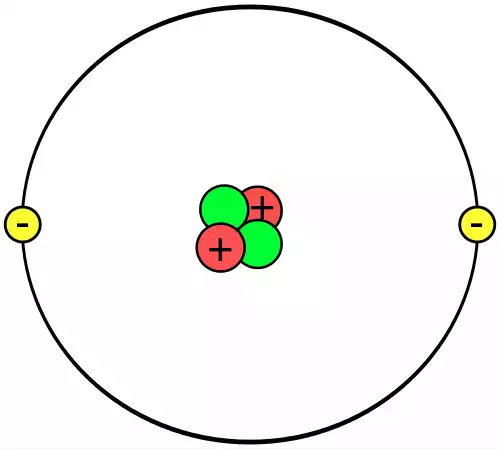
هسته و الکترونهای هستهای یک اتم، هسته اتم را تشکیل میدهند. الکترونهای هستهای با نیروی خیلی قوی به هسته متصل هستند. بنابراین، بر عکس الکترونهای ظرفیت، الکترونهای هستهای باجداسازی بار مثبت هسته اتم از الکترونهای ظرفیت نقش ثانویهای در پیوند و واکنشهای شیمیایی بازی میکنند. تعداد الکترونهای ظرفیتی یک عنصر میتواند با توجه به گروه جدول تناوبی آن عنصر تعیین شود (برای اطلاعات بیشتر به الکترون ظرفیتی مراجعه کنید).